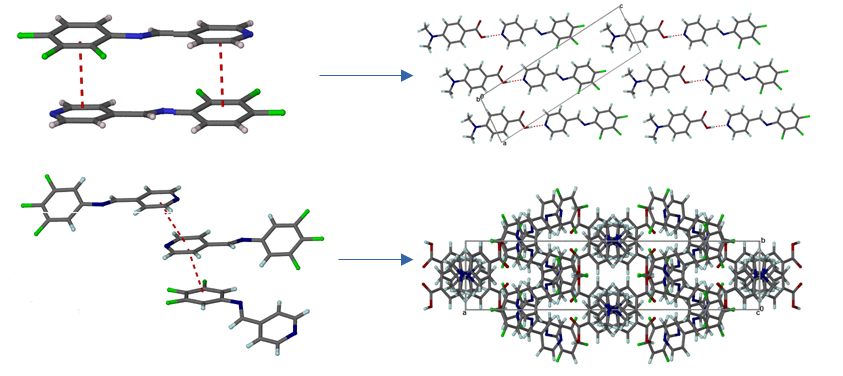
Influence of Fluorine Substitution on π-π Stacking and Molecular Packing in Schiff Base Cocrystals
DOI:
https://doi.org/10.29356/jmcs.v70i1.2508Keywords:
Cocrystal, π-π interactions, H-bonding, Hirshfeld surface, influence of F atomsAbstract
In this study, we investigate the role of fluorine atom positioning in the supramolecular organization, π-π stacking interactions, and molecular packing of Schiff base cocrystals. Three cocrystals, each containing (E)-N-(trifluoroaniline)-1-(4-pyridinyl)-methanimine with p-dimethylaminobenzoic acid, were synthesized with fluorine atoms positioned at different sites on the aromatic rings (2,3,4; 2,4,5; and 3,4,5). IR spectroscopy confirmed the formation of cocrystals, highlighting the presence of strong O−H···N hydrogen bonds. Crystal structure analysis revealed that fluorination at the 2,3,4 positions led to parallel molecular packing, whereas fluorination at the 2,4,5 and 3,4,5 positions resulted in oblique-angle packing. Hirshfeld surface analysis and density functional theory (DFT) calculations demonstrated that π-π interactions, particularly between the pyridine and trifluorinated aromatic rings, are energetically significant and often surpass the strength of hydrogen bonds. These findings underscore the importance of fluorine atom positioning in determining the molecular packing and provide valuable insights into the design of cocrystals through the strategic manipulation of intermolecular forces.
Resumen. En este estudio investigamos el papel de la posición de los átomos de flúor en la organización supramolecular, las interacciones de apilamiento π-π y el empaquetamiento molecular de cocristales de una base de Schiff. Tres cocristales, cada uno conteniendo (E)-N-(trifluoroanilina)-1-(4-piridinil)-metanimina con ácido p-dimetilaminobenzóico, fueron sintetizados con átomos de flúor posicionados en diferentes sitios de los anillos aromáticos (2,3,4; 2,4,5; y 3,4,5). La espectroscopía IR confirmó la formación de cocristales, destacando la presencia de fuertes enlaces de hidrógeno O−H···N. El análisis de las estructuras cristalinas reveló que el patrón de fluoración en las posiciones 2,3,4 condujo a un empaquetamiento molecular paralelo, mientras que la fluoración en las posiciones 2,4,5 y 3,4,5 resultó en arreglos de empaquetamiento oblicuos. El análisis de superficie de Hirshfeld y los cálculos con la teoría del funcional de la densidad (DFT) demostraron que las interacciones π-π, en particular entre la piridina y los anillos aromáticos trifluorados, son energéticamente significativas y, a menudo, superan la fuerza de los enlaces de hidrógeno. Estos hallazgos resaltan la importancia de la posición de los átomos de flúor en la determinación del empaquetamiento molecular y ofrecen información valiosa para el diseño de cocristales mediante la manipulación estratégica de las fuerzas intermoleculares.
Downloads
References
1. Karimi-Jafari, M.; Padrela, L.; Walker, G.M.; Croker, D.M. Cryst. Growth Des. 2018, 18, 10, 6370–6387. DOI: https://doi.org/10.1021/acs.cgd.8b00933.
2. Li, S., Cooper, V.R.; Thonhauser, T.; Lundqvist, B.I.; Langreth, D.C. J. Phys. Chem. B. 2009, 113, 11166–11172. DOI: https://doi.org/10.1021/JP905765C.
3. Carter-Fenk, K.; Liu, M.; Pujal, L.; Loipersberger, M.; Tsanai, M.; Vernon, R.M.; Forman-Kay, J.D.; Head-Gordon, M.; Heidar-Zadeh, F.; Head-Gordon, T. J. Am. Chem. Soc. 2023, 145, 24836–24851. DOI: https://doi.org/10.1021/JACS.3C09198.
4. McGaughey, G.B.; Gagné, M.; Rappé, A.K. J. Biol. Chem. 1998, 273, 15458–15463. DOI: https://doi.org/10.1074/jbc.273.25.15458.
5. Tiekink, E.R.T.; Zukerman-Schpector, J., in: The Importance of Pi‐Interactions in Crystal Engineering, Wiley, 2012. DOI: https://doi.org/10.1002/9781119945888.
6. Jaime-Adán, E.; Hernández-Ortega, S.; Toscano, R.A.; Germán-Acacio, J.M.; Sánchez-Pacheco, A.D.; Hernández-Vergara, M.; Barquera, J.E.; Valdés-Martínez, J. Cryst. Growth. Des. 2024, 24, 1888–1897. DOI: https://doi.org/10.1021/acs.cgd.3c00910.
7. Ojala,W.H.; Arola,T.M.; Herrera, N.; Balidemaj, B.; Ojala,C.R. Acta Crystallogr. C. 2007, 63, o207–o211. DOI: https://doi.org/10.1107/S0108270107006233.
8. Ojala, W.H.; Smieja, J.M.; Spude, J.M.; Arola, T.M.; Kuspa, M.K.; Herrera, N. Acta Crystallogr. B. 2007 63 485–496. DOI: https://doi.org/10.1107/S0108768107018034.
9. Ojala, W.H.; Lystad, K.M.; Deal, T.L.; Engebretson, J.E.; Spude, J.M.; Balidemaj, B.; Ojala, C.R. Cryst. Growth. Des. 2009, 9 964–970. DOI: https://doi.org/10.1021/cg8007443.
10. MacGillivray, L.R. J. Org. Chem. 2008, 73, 3311–3317. DOI: https://doi.org/10.1021/jo8001563.
11. Sinnwell, M. A.; Baltrusaitis, J.; MacGillivray, L.R. Cryst. Growth. Des. 2015, 15, 538–541. DOI: https://doi.org/10.1021/cg501571u.
12. Li, C.; Campillo-Alvarado, G.; Swenson, D.C.; MacGillivray, L.R. CrystEngComm. 2021, 23, 1071–1074. DOI: https://doi.org/10.1039/D0CE01885F.
13. Bučar, D.-K.; Sen, A.; Mariappan, S.V.S.; MacGillivray, L.R. Chem. Comm. 2012, 48 1790. DOI: https://doi.org/10.1039/c2cc15453f.
14. Sinnwell, M.A.; Groeneman, R.H.; Ingenthron, B.J.; Li, C.; MacGillivray, L.R. Commun Chem. 2021, 4, 60. DOI: https://doi.org/10.1038/s42004-021-00493-3.
15. Grobelny, A.L.; Rath, N.P.; Groeneman, R.H., CrystEngComm. 2018, 20, 3951–3954. DOI: https://doi.org/10.1039/C8CE00447A.
16. Mondal, B.; Zhang, T.; Prabhakar, R.; Captain, B.; Ramamurthy, V. Photochem. Photobiol. 2014, 13,1509–1520. DOI: https://doi.org/10.1039/c4pp00221k.
17. Hu, F.; Mi, Y.; Zhu, C.; Abrahams, B.F.; Braunstein, P.; Lang, J. Angew. Chem., Int. Ed. Engl. 2018, 130, 12878–12883. DOI: https://doi.org/10.1002/ANGE.201806076.
18. Präsang, C.; Nguyen, H.L.; Horton, P.N.; Whitwood, A.C.; Bruce, D.W. Chem. Comm. 2008, 6164. DOI: https://doi.org/10.1039/b811716k.
19. Cariati, E.; Roberto, D.; Ugo, R.; Srdanov, V.I.; Galli, S.; Macchi, V; Sironi, A. New J. Chem. 2002, 26 13–15. DOI: https://doi.org/10.1039/b107632a.
20. Wong, J.P.‐W.; Whitwood, A.C.; Bruce, D.W. Chem. Eur. J. 2012, 18, 16073–16089. DOI: https://doi.org/10.1002/chem.201201906.
21. Bruce, D.W.; Metrangolo, P.; Meyer, F.; Präsang, C.; Resnati, G.; Terraneo, G.; Whitwood, A.C. New J. Chem. 2008, 32, 477–482. DOI: https://doi.org/10.1039/B709107A.
22. Jaime-Adán, E.; Germán-Acacio, J.M.; Toscano, R.A.; Hernández-Ortega, S.; Valdés-Martínez, J. Cryst. Growth. Des. 2020, 20, 2240–2250. DOI: https://doi.org/10.1021/acs.cgd.9b01371.
23. Jaime-Adán, E.; Hernández-Ortega, S.; Toscano, R.A.; Germán-Acacio, J.M.; Sánchez-Pacheco, A.D.; Hernández-Vergara, M.; Barquera, J.E.; Valdés-Martínez, J. Cryst. Growth. Des. 2024, 24, 1888–1897. DOI: https://doi.org/10.1021/acs.cgd.3c00910.
24. Sánchez-Pacheco, A.D.; Hernández-Vergara, M.; Jaime-Adán, E.; Hernández-Ortega,V; Valdés-Martínez, J. J Mol Struct 2021, 1234. DOI: https://doi.org/10.1016/j.molstruc.2021.130136.
25. Bruker AXS Inc; APEX 3, SAINT and SADABS, Wisconcin, Madison, USA, 2007.
26. Sheldrick, G.M. Acta Crystallogr. Section A. 2015 71 3–8. DOI: https://doi.org/10.1107/S2053273314026370.
27. Sheldrick, G.M. Acta Crystallogr. C Struct. Chem. 2015, 71, 3–8. DOI: https://doi.org/10.1107/S2053229614024218.
28. Spek, A.L. J. Appl. Crystallogr. 2003, 36, 7–13. DOI: https://doi.org/10.1107/S0021889802022112.
29. Macrae, C.F.; Sovago, I.; Cottrell, S.J., Galek, P.T.A.; McCabe, P.; Pidcock, E.; Platings, M.; Shields, G.P.; Stevens, J.S.; Towler, M.; Wood, P.A. J. Appl. Crystallogr. 2020, 53 226–235. DOI: https://doi.org/10.1107/S1600576719014092.
30. Barbour, L.J. J. Appl. Crystallogr. 2020, 53, 1141–1146. DOI: https://doi.org/10.1107/S1600576720007438.
31. Spackman, P.R.; Turner, M.J.; McKinnon, J.J.; Wolff, S.K.; Grimwood, D.J.; Jayatilaka, D.; Spackman, M.A. 2021, 54, 1006–1011. DOI: https://doi.org/10.1107/S1600576721002910.
32. Spackman, M.A.; Jayatilaka, D.; CrystEngComm. 2009, 11, 19–32. DOI: https://doi.org/10.1039/b818330a.
33. Spackman, M.A.; McKinnon, J.J. CrystEngComm. 2002, 4, 378–392. DOI: https://doi.org/10.1039/b203191b.
34. Gavezzotti, A. Acc. Chem. Res. 1994, 27, 309–314. DOI: https://doi.org/10.1021/ar00046a004.
35. Gavezzotti, A.; Filippini, G. J. Phys. Chem. 2002, 98 4831–4837. DOI: https://doi.org/10.1021/J100069A010.
36. Aakeröy, C.B.; Rajbanshi, A.; Li, Z.J.; Desper, J. CrystEngComm. 2010, 12, 4231. DOI: https://doi.org/10.1039/c0ce00052c.
37. Brittain, H.G. Cryst. Growth. Des. 2009, 9, 2492–2499. DOI: https://doi.org/10.1021/cg801397t.
38. Childs, S.L.; Stahly, V.; Park, A. Mol. Pharm. 2007, 4, 323–338. DOI: https://doi.org/10.1021/mp0601345.
39. da Silva, C.C.; Guimarães, F.F.; Ribeiro, L.; Martins, V. Spectrochim. Acta A Mol. Biomol. Spectrosc. 2016, 167, 89–95. DOI: https://doi.org/10.1016/j.saa.2016.05.042.

Downloads
Published
Issue
Section
License
Copyright (c) 2026 Mónica Hernández-Vergara, Addi Dana Sánchez-Pacheco, Simón Hernández-Ortega, Jesús Valdés-Martínez

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.