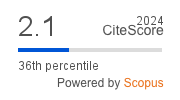
Pentalinon andrieuxii, a Medicinal Plant with Antiviral Activity Against the Influenza A(H1N1pdm09) Virus
DOI:
https://doi.org/10.29356/jmcs.v70i1.2494Keywords:
cytopathic effect, Apocynaceae, Influenza, PolyphenolicsAbstract
Respiratory viral infections, including influenza, continue to pose a significant global health challenge, leading to seasonal epidemics every year. The 2009 outbreak, triggered by a new strain of the influenza A(H1N1pdm09) virus, marked the first influenza pandemic of the 21st century that resulted in over 200,000 fatalities across more than 214 countries. Presently, and despite the availability of vaccines and antiviral medications, the ongoing mutations of these viruses necessitates continuing the search for new and more effective antiviral treatments.
Pentalinon andrieuxii, a vine native to the Yucatán Península, is traditionally used in Mayan medicine to treat snake bites and the skin lesions caused by cutaneous leishmaniasis. Current phytochemical knowledge of P. andrieuxii includes reports of tri-nor-sesquiterpenes, triterpenes, steroid derivatives, and sterols. However, to date, there are no reports on the antiviral activity of the extract or secondary metabolites from this plant. As part of our search for new antiviral metabolites from plants of the Apocynaceae family, we wish to report herein on the inhibition of the cytopathic effect of the semipurified fractions from the leaf extract of P. adrieuxii, when tested against the A/Yucatan/2370/09 (H1N1pdm09) strain of the influenza A virus, and the identification of polyphenolic metabolites in the bioactive fraction.
Resumen. Las infecciones respiratorias causadas por virus, entre ellas la gripe, siguen siendo un importante reto sanitario a nivel mundial, cada año provocan epidemias estacionales. El brote de 2009, desencadenado por una nueva cepa del virus de la gripe A(H1N1pdm09), marcó la primera pandemia de gripe del siglo XXI y causó más de 200,000 víctimas mortales en más de 214 países. En la actualidad, pese a la disponibilidad de vacunas y medicamentos antivirales, las continuas mutaciones de estos virus obligan a seguir buscando tratamientos antivirales nuevos y más eficaces.
Pentalinon andrieuxii, una enredadera originaria de la Península de Yucatán, se utiliza tradicionalmente en la medicina maya para tratar las mordeduras de serpiente y las lesiones cutáneas causadas por la leishmaniasis cutánea. El conocimiento fitoquímico actual de P. andrieuxii incluye informes de tri-nor-sesquiterpenos, triterpenos, derivados de esteroides y esteroles. Sin embargo, hasta la fecha no existen informes sobre la actividad antiviral del extracto o los metabolitos secundarios de esta planta. Como parte de nuestra búsqueda de nuevos metabolitos antivirales de plantas de la familia Apocynaceae, deseamos reportar la inhibición del efecto citopático de fracciones semipurificadas del extracto de hoja de P. andrieuxii, evaluados contra la cepa A/Yucatan/2370/09 (H1N1pdm09) del virus de Influenza A, y la identificación de polifenoles en la fracción bioactiva.
Downloads
References
1. Rajão, D. S.; Pérez, D. R. Front. Microbiol. 2018 9. DOI: https://doi.org/10.3389/fmicb.2018.00123.
2. Alirol, E.; Getaz, L.; Stoll, B.; Chappuis, F.; Loutan, L. Lancet Infect. Dis. 2011, 11, 131–141. DOI: https://doi.org/10.1016/s1473-3099(10)70223-1.
3. Kapiriri, L.; Ross, A. Glob. Soc. Welf. 2020, 7, 33–45. DOI: https://doi.org/10.1007/s40609-018-0123-y.
4. Eisfeld, A. J.; Neumann, G.; Kawaoka, Y. Nat. Rev. Microbiol. 2015, 13, 28–41. DOI: https://doi.org/10.1038/nrmicro3367.
5. Lowen, A. C.; Steel, J.; Schultz-Cherry, S. J. Virol. 2014, 88, 7692–7695. DOI: https://doi.org/doi:10.1128/JVI.03544-13.
6. Chaudhuri, S.; Symons, J. A.; Deval, J. Antivir. Res. 2018, 155, 76–88. DOI: https://doi.org/10.1016/j.antiviral.2018.05.005.
7. Shin, W.-J.; Seong, B. L. Expert Opin. Drug Discov. 2019, 14, 153–168. DOI: https://doi.org/10.1080/17460441.2019.1560261.
8. Miresmailli, S.; Isman, M. B. Trends Plant Sci. 2014, 19, 29–35. DOI: https://doi.org/10.1016/j.tplants.2013.10.002.
9. Perez, R. M. Pharm. Biol. 2003 41, 107–157. DOI: https://doi.org/10.1076/phbi.41.2.107.14240.
10. Yadav, K.; Divyadeepika; Joshi, J. Mater. Today Proc. 2024. DOI: https://doi.org/10.1016/j.matpr.2024.04.003.
11. Villegas Acosta, I. F. El papel de los cardenólidos en la interacción Pentalinon andrieuxii–Syntomeida epilais y su efecto en la metilación del ADN del insecto como estrategia ecológica de conservación; Tesis de Maestría, Centro de Investigación Científica de Yucatán: Mérida, Yucatán, México 2019.
12. Pan, L.; Lezama-Davila, C. M.; Isaac-Marquez, A. P.; Calomeni, E. P.; Fuchs, J. R.; Satoskar, A. R.; Kinghorn, A. D. Phytochemistry 2012, 82, 128–135. DOI: https://doi.org/10.1016/j.phytochem.2012.06.012.
13. Newman, R. A.; Sastry, K. J.; Arav-Boger, R.; Cai, H.; Matos, R.; Harrod, R. J. Exp. Pharmacol. 2020 503–515. DOI: https://doi.org/10.2147/JEP.S273120.
14. Williams, R. S.; Benkeblia, N. Sci. Hortic. 2018, 236, 36–42. DOI: https://doi.org/10.1016/j.scienta.2018.03.007.
15. Huber, G. M.; Rupasinghe, H. P. V. J. Food Sci. 2009, 74, C693–C700. DOI: https://doi.org/10.1111/j.1750-3841.2009.01356.x.
16. Covarrubias-Cárdenas, A.; Patrón-Vázquez, J.; Espinosa-Andrews, H.; Ayora-Talavera, T.; García-Cruz, U.; Pacheco, N. J. Food Sci. Technol. 2018, 55, 5106–5114. DOI: https://doi.org/10.1007/s13197-018-3451-0.
17. Chan-Bacab, M. J.; Balanza, E.; Deharo, E.; Muñoz, V.; Durán-García, R.; Peña-Rodríguez, L. M. J. Ethnopharmacol. 2003, 86, 243–247. DOI: https://doi.org/10.1016/S0378-8741(03)00011-4.
18. Fields, B.; Knipe, D.; Howley, P. Fields’ Virology; Lippincott Williams & Wilkins: Philadelphia 2007.
19. Suchman, E.; Blair, C. Cytopathic Effects of Viruses: Protocols 2007.
20. Kim, M.; Nguyen, D. V.; Heo, Y.; Park, K. H.; Paik, H. D.; Kim, Y. B. J. Microbiol. Biotechnol. 2020, 30, 172–177. DOI: https://doi.org/10.4014/jmb.1908.08001.
21. Chojnacka, K.; Skrzypczak, D.; Izydorczyk, G.; Mikula, K.; Szopa, D.; Witek-Krowiak, A. Foods 2021, 10, 2277. DOI: https://doi.org/10.3390/foods10102277.
22. Surco Laos, F.; Ayquipa Paucar, H.; Quispe Gamboa, W.; García Ceccarelli, J.; Valle Campos, M. Rev. Soc. Quím. Perú 2020, 86, 123–131. DOI: https://doi.org/10.37761/rsqp.v86i2.
23. Kamboj, A.; Saluja, A. K.; Kumar, M.; Atri, P. J. Pharm. Res. 2012, 5, 2402–2412.
24. Álvarez, E.; Jiménez, O.; Posada, C.; Rojano, B.; Gil, J.; García, C.; Durango, D. Vitae 2008, 15, 165–172.
25. Montufar-Canto, D. A.; González Salvatierra, C.; Hernández-Chávez, L. I.; Uc-Cachón, A. H.; Molina-Salinas, G. M. Trop. Subtrop. Agroecosyst. 2025 28. DOI: http://doi.org/10.56369/tsaes.5364.
26. Garayar Flores, R. C.; Chávez Orellana, H. Rev. Peru. Med. Integr. 2016, 1, 31–37. DOI: https://doi.org/10.26722/rpmi.2016.14.33.
27. Barthwal, R.; Mahar, R. Metabolites 2024, 14, 119. DOI: https://doi.org/10.3390/metabo14020119.
28. Jamal, Q. M. S.; Ahmad, V. Pharm. 2024, 17, 450. DOI: https://doi.org/10.3390/ph17040450.
29. Kaul, T. N.; Middleton, E., Jr.; Ogra, P. L. J. Med. Virol. 1985, 15, 71–79. DOI: https://doi.org/10.1002/jmv.1890150110.
30. Ninfali, P.; Antonelli, A.; Magnani, M.; Scarpa, E. S. Nutrients 2020 12. DOI: https://doi.org/10.3390/nu12092534.
31. Li, R.; Narita, R.; Nishimura, H.; Marumoto, S.; Yamamoto, S. P.; Ouda, R.; Yatagai, M.; Fujita, T.; Watanabe, T. ACS Sustainable Chem. Eng. 2018, 6, 119–126. DOI: https://doi.org/10.1021/acssuschemeng.7b01265.

Downloads
Published
Issue
Section
License
Copyright (c) 2026 Ismael Fernando Villegas-Acosta, Guadalupe Ayora-Talavera, Neith Pacheco-López, Iván Emanuel Herrera-Pool, Karlina García-Sosa, Luis Manuel Peña-Rodríguez

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.