Thymol-Loaded Chitosan Nanoparticles: A New Ionic Gelation Method Using a Venturi Tube
DOI:
https://doi.org/10.29356/jmcs.v70i1.2467Keywords:
Venturi tube, thymol, chitosan, nanoparticles, ionic gelation, mixerAbstract
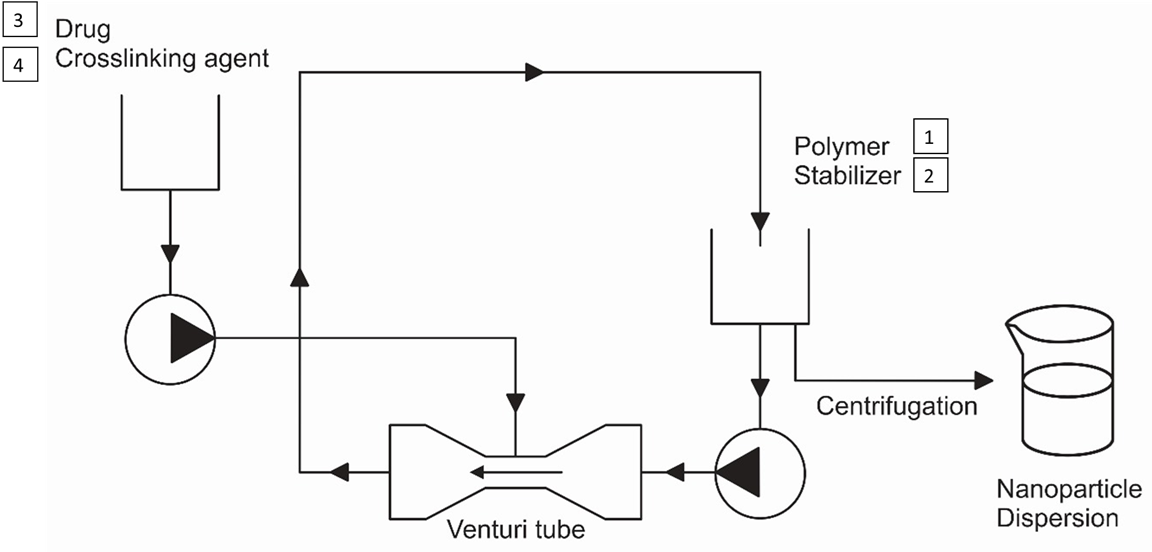
This study aimed to explore the potential of the Venturi tube as an innovative and scalable platform for preparing thymol-loaded chitosan nanoparticles (Tym-Ch-NP´s) using the ionic gelation method. Chitosan and thymol was used as polymer and bioactive compound, respectively. Unlike conventional processes, the Venturi tube provides continuous and efficient mixing, enhancing mass transfer and process reproducibility, which are key challenges in nanoparticle production. The effects of recirculation rate, stabilizing and crosslinking agent concentrations were evaluated. The systems obtained showed particle size around of ~ 300 nm, polydispersity index ~ 0.3 and zeta potential ~ +30 mV. Encapsulation efficiency ranged from 18.5 to 67.5 %. The highest efficiency was obtained under the following conditions: stabilizer 3.0 % (w/v), tripolyphosphate 0.5 % (w/v) and recirculation rate 5.8 L/min. The transmission and backscattering profiles verified that the nanoparticles prepared showed slight flocculation, with a DBS < 10 %, but are considered stable due to their zeta potential. These findings highlight the novelty and importance of adapting the Venturi tube to ionic gelation, demonstrating its capacity to produce stable nanoparticles and include model drug with potential application in the pharmaceutical chemical industry in a reproducible and scalable manner.
Resumen. El principal objetivo de este estudio fue explorar el potencial del tubo Venturi como una plataforma innovadora y escalable en la preparación de nanopartículas de quitosano cargadas con timol usando el método de gelación iónica. Para este método se utilizó quitosano como polímero y timol como compuesto bioactivo. A diferencia de los sistemas convencionales por lote, el tubo Venturi proporciona una mezcla continua y eficiente, mejorando la transferencia de masa y la reproducibilidad del proceso, que representan desafíos clave en la producción de nanopartículas. Los resultados demostraron el efecto de la velocidad de recirculación, concentración del estabilizante y agente de entrecruzamiento. El tamaño de partícula obtenido fue de ~ 300 nm, el índice de polidispersidad de ~ 0.3 y el potencial zeta de ~ + 30 mV. La eficiencia de encapsulación fue de 18.5 a 67.5 %. La mejor eficiencia de encapsulación se obtuvo empelando: estabilizante al 3.0 % (p/v), tripolifosfato 0.5 % (p/v) y una velocidad de recirculación de 5.8 L/min. Los perfiles de retrodispersión de luz mostraron una leve floculación con un valor de ABS menor al 10 %, pero es considerado estable debido a su valor de potencial zeta. Estos hallazgos destacan la novedad e importancia de la adaptación de la metodología del tubo Venturi a la de gelación iónica, demostrando su capacidad para producir nanopartículas estables y encapsular compuestos bioactivos con potencial aplicación en la industria química farmacéutica de manera reproducible y escalable.
Downloads
References
1. Grzywacz, R. Czas. Tech. 2017, 11, 95–106. DOI: https://doi.org/10.4467/2353737xct.17.192.7421.
2. García-Salazar, G.; Zambrano-Zaragoza, M. L.; Quintanar-Guerrero, D. Int. J. Pharm. 2018, 545, 254–260. DOI: https://doi.org/10.1016/j.ijpharm.2018.05.005.
3. García-Salazar, G.; Zambrano-Zaragoza, M. de la L.; Serrano-Mora, E.; Mendoza-Díaz, S. O.; Leyva-Gomez, G.; Quintanar-Guerrero, D. Drug Dev. Ind. Pharm. 2021, 47, 1302–1309. DOI: https://doi.org/10.1080/03639045.2021.1989456.
4. Morin-Crini, N.; Lichtfouse, E.; Torri, G.; Crini, G. Environ. Chem. Lett. 2019, 17, 1667–1692. DOI: https://doi.org/10.1007/s10311-019-00904-x.
5. Singh, A.; Mittal, A.; Benjakul, S. ScienceAsia. 2021, 47, 1–10. DOI: https://doi.org/10.2306/scienceasia1513-1874.2021.020.
6. Llana-Ruiz-Cabello, M.; Pichardo, S.; Maisanaba, S.; Puerto, M.; Prieto, A. I.; Gutiérrez-Praena, D.; Jos, A.; Cameán, A. M. Food Chem. Toxicol. 2015, 81, 9–27. DOI: https://doi.org/10.1016/j.fct.2015.03.030.
7. Kunjachan, S.; Jose, S. Asian J. Pharm. 2010, 4, 148–153. DOI: https://doi.org/10.4103/0973-8398.68467.
8. Çakır, M. A.; Icyer, N. C.; Tornuk, F. Int. J. Biol. Macromol. 2020, 151, 230–238. DOI: https://doi.org/10.1016/j.ijbiomac.2020.02.096.
9. Oluoch, G.; Matiru, V.; Mamati, E. G.; Nyongesa, M. Adv. Microbiol. 2021, 11, 723–739. DOI: https://doi.org/10.4236/aim.2021.1112052.
10. Sullivan, D. J.; Cruz-Romero, M.; Collins, T.; Cummins, E.; Kerry, J. P.; Morris, M. A. Food Hydrocoll. 2018, 83, 355–364. DOI: https://doi.org/10.1016/j.foodhyd.2018.05.010.
11. Yoksan, R.; Jirawutthiwongchai, J.; Arpo, K. Colloids Surf., B. 2010, 76, 292–297. DOI: https://doi.org/10.1016/j.colsurfb.2009.11.007.
12. Sundararaj, S.; Selladurai, V. Arab. J. Sci. Eng. 2013, 38, 3563–3573. DOI: https://doi.org/10.1007/s13369-013-0643-9.
13. Shayeganfar, F.; Javidpour, L.; Taghavinia, N.; Tabar, M. R. R.; Sahimi, M.; Bagheri-Tar, F. Phys. Rev. 2010, 81, 026304-8. DOI: https://doi.org/10.1103/PhysRevE.81.026304.
14. Medina, E.; Caro, N.; Abugoch, L.; Gamboa, A.; Díaz-Dosque, M.; Tapia, C. J. Food Eng. 2019, 240, 191–198. DOI: https://doi.org/10.1016/j.jfoodeng.2018.07.023.
15. Masalova, O.; Kulikouskaya, V.; Shutava, T.; Agabekov, V. Phys. Procedia. 2013, 40, 69–75. DOI: https://doi.org/10.1016/j.phpro.2012.12.010.
16. Rajaram, S.; Natham, R. Res. J. Pharm. Biol. Chem. Sci. 2013, 4, 820–832.
17. Danaei, M.; Dehghankhold, M.; Ataei, S.; Hasanzadeh Davarani, F.; Javanmard, R.; Dokhani, A.; Khorasani, S.; Mozafari, M. R. Pharmaceutics. 2018, 10. DOI: https://doi.org/10.3390/pharmaceutics10020057.
18. Al-Nemrawi, N. K.; Alsharif, S. S. M.; Dave, R. H. Int. J. Appl. Pharm. 2018, 10, 60–65. DOI: https://doi.org/10.22159/ijap.2018v10i5.26375.
19. Escalona-Rayo, O.; Fuentes-Vázquez, P.; Jardon-Xicotencatl, S.; García-Tovar, C. G.; Mendoza-Elvira, S.; Quintanar-Guerrero, D. J. Drug Deliv. Sci. Technol. 2019, 52, 488–499. DOI: https://doi.org/10.1016/j.jddst.2019.05.026.
20. Algharib, S. A.; Dawood, A.; Zhou, K.; Chen, D.; Li, C.; Meng, K.; Zhang, A.; Luo, W.; Ahmed, S.; Huang, L.; et al. J. Mol. Struct. 2022, 1252, 132129. DOI: https://doi.org/10.1016/j.molstruc.2021.132129.
21. Bangun, H.; Tandiono, S.; Arianto, A. J. Appl. Pharm. Sci. 2018, 8, 147–156. DOI: https://doi.org/10.7324/JAPS.2018.81217.
22. Essid, R.; Ayed, A.; Djebali, K.; Saad, H.; Srasra, M.; Othmani, Y.; Fares, N.; Jallouli, S.; Abid, I.; Rashed, M.; et al. Molecules. 2023, 28, 5681. DOI: https://doi.org/10.3390/molecules28155681.
23. Gokce, Y.; Cengiz, B.; Yildiz, N.; Calimli, A.; Aktas, Z. Colloids Surfaces A. 2014, 462, 75–81. DOI: https://doi.org/10.1016/j.colsurfa.2014.08.028.
24. Boge, L.; Västberg, A.; Umerska, A.; Bysell, H.; Eriksson, J.; Edwards, K.; Millqvist-Fureby, A.; Andersson, M. J. Colloid Interface Sci. 2018, 522, 126–135. DOI: https://doi.org/10.1016/j.jcis.2018.03.062.
25. Fernandez-De arlas, B.; Gómez, S.; Corcuera, M.-A.; Eceiza, A. Rev. Iberoam. Polim. 2014, 15, 211–218.
26. de Chasteigner, S.; Cavé, G.; Fessi, H.; Devissaguet, J.-P.; Puisieus, F. Drug Dev. Res. 1996, 38, 116–124.
27. Raikos, V. Food Hydrocoll. 2017, 72, 155–162. DOI: https://doi.org/10.1016/j.foodhyd.2017.05.027.
28. Kaombe, D. D.; Lenes, M.; Toven, K.; Glomm, W. R. Energy Fuels. 2013, 27, 1446–1452. DOI: https://doi.org/10.1021/ef302121r.
29. Mengual, O.; Meunier, G.; Cayré, I.; Puech, K.; Snabre, P. Talanta. 1999, 50, 445–456. DOI: https://doi.org/10.1016/S0039-9140(99)00129-0.
30. González-Reza, R. M.; Quintanar-Guerrero, D.; Del Real-López, A.; Piñon-Segundo, E.; Zambrano-Zaragoza, M. L. LWT - Food Sci. Technol. 2018, 90, 354–361. DOI: https://doi.org/10.1016/j.lwt.2017.12.044.
31. Santonocito, D.; Sarpietro, M. G.; Carbone, C.; Panico, A.; Campisi, A.; Siciliano, E. A.; Sposito, G.; Castelli, F.; Puglia, C. Molecules. 2020, 25. DOI: https://doi.org/10.3390/molecules25132991.

Downloads
Published
Issue
Section
License
Copyright (c) 2026 Gilberto Garcia-Salazar, Diego Francisco Romero-Alatorre, Maria de la Luz Zambrano-Zaragoa, Luis Eduardo Serrano-Mora, Gustavo Vidal-Romero, David Quintanar-Guerrero

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.