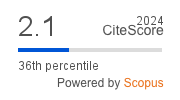
Tri-Organotin(IV) Coordination Compounds Derived from a Cholesteryl Dithiophosphonate Ligand. Synthesis, Characterization, Structure, and Antibacterial Evaluation
DOI:
https://doi.org/10.29356/jmcs.v70i1.2489Keywords:
Dithiophosphonates, cholesteryl complexes, organotin, X-ray single crystal, complex biological activityAbstract
Among the dithio-organophosphorus metal coordination compounds, dithiophosphonates have received significantly less attention than dithiophosphates and dithiophosphinates. This is partly due to the inherent difficulties in synthesizing phosphonates. Herein, we report the synthesis and characterization of four new organotin(IV) dithiophosphonate coordination compounds, bearing an O-cholesteryl substituent on phosphorus: [Me3Sn{S2P(O-cholesteryl)(4-MeOC6H4)}] (2), [Bu3Sn{S2P(O-cholesteryl)(4-MeOC6H4)}] (3), [Cy3Sn{S2P(O-cholesteryl)(4-MeOC6H4)}] (4), [Ph3Sn{S2P(O-cholesteryl)(4-MeOC6H4)}] (5). These compounds were obtained through the reaction between the triethylammonium salt of O-3-b-cholest-5-en-3-yl)(4-methoxyphenyl)dithiophosphonate (1) and the corresponding triorganotin(IV) chlorides. The compounds were characterized using elemental analysis, IR spectroscopy, and NMR spectroscopy (1H, 13C, 31P, and 119Sn). Infrared spectra (solid-state) suggest that the Sn(IV) is coordinated in an anisobidentate mode. In solution, the 119Sn NMR chemical shifts indicate tetracoordination for 2 and 4 and pentacoordination for 3 and 5. Single-crystal X-ray analysis of 5 revealed an anisobidentate coordination mode of the dithiophosphonate and a highly distorted trigonal bipyramidal geometry around Sn(IV), closer to a trigonal bipyramid than to a square pyramid. The phosphorus atom is chiral and adopts the relative configuration R. The antibacterial test indicates that compound 5 exhibits antibacterial activity, while the others show no inhibition against any of the bacterial strains used.
Resumen. Dentro de los compuestos metálicos de coordinación conteniendo ligantes ditio-organofosforados, los ditiofosfonatos han recibido significativamente mucha menos atención que los bien estudiados ditiofosfinatos y ditiofosfatos. Lo anterior es parcialmente debido a las inherentes mayores dificultades sintéticas de los ditiofosfonatos. En esta investigación informamos la síntesis y caracterización de cuatro nuevos compuestos de coordinación de organoestaño(IV) con un ligante ditiofosfonato, conteniendo O-colesterilo. Los compuestos de organoestaño (IV) sintetizados son: [Me3Sn{S2P(O-colesteril)(4-MeOC6H4)}] (2), [Bu3Sn{S2P(O-colesteril)(4-MeOC6H4)}] (3), [Cy3Sn{S2P(O-colesteril)(4-MeOC6H4)}] (4), [Ph3Sn{S2P(O-colesteril)(4-MeOC6H4)}] (5). La síntesis se llevó a cabo a través de la reacción entre la sal de trietilamonio del O-3-b-colest-5-en-3-yl)(4-metoxifenil)ditiofosfonato (1) y los correspondientes cloruros de triorganoestaño(IV). Los compuestos obtenidos fueron caracterizados por análisis elemental, espectroscopia IR y RNM (1H, 13C, 31P, y 119Sn). Los espectros infrarrojos (estado sólido) sugieren que el Sn(IV) se encuentra coordinado al ligante en un modo anisobidentado, mientras que en solución los desplazamientos químicos de 119Sn RNM indican tetracoordinación para 2 y 4 y pentacoordinación para 3 y 5. El análisis por rayos X de monocristal de 5 revela un modo de coordinación anisobidentado del ditiofosfonato y una geometría trigonal bipiramidal altamente distorsionada alrededor del Sn(IV), la cual es más cercana a una bipirámide trigonal que a una pirámide cuadrada, donde el átomo de fósforo es quiral y asume la configuración relativa R. Las pruebas antibacterianas indican que el compuesto 5 exhibe actividad antibacteriana, mientras que los demás no muestran inhibición contra ninguna de las cepas utilizadas.
Downloads
References
1. (a) Haiduc, I.; Sowerby, D.B. Polyhedron. 1995, 15, 2469-2521. DOI: https://doi.org/10.1016/0277-5387(95)00554-4. (b) Haiduc, I.; Sowerby, D.B.; Lu, S-F. Polyhedron. 1995, 14, 3389-3472. DOI: https://doi.org/10.1016/0277-5387(95)00108-5.
2. (a) Haiduc, I. J. Organomet. Chem. 2001, 623, 298-42. DOI: https://doi.org/10.1016/S0022-328X(00)00677-X. (b) Semeniuc, R.F.; Baum, R.R.; Veach, J.J.; Wheeler, K.A.; Pellechia, P.J. Inorg. Chim. Acta 2013, 400, 228-238. DOI: https://doi.org/10.1016/j.ica.2013.02.037.
3. van Zyl, W.E.; Woollins, J.D. Coord. Chem. Rev. 2013, 257, 718-731. DOI: https://doi.org/10.1016/j.ccr.2012.10.010.
4. (a) Yusuf, T.L.; Ogundare, S. A.; Pillay, M. N.; van Zyl, W.E. Molecules. 2022, 27, 5223. DOI: https://doi.org/10.3390/molecules27165223. (b) Jangid, D.K.; Dastider, S.G.; Biswas, R.; Khirid, S.; Meena, S.; Kumar, P.; Sahoo, S.C.; Verma, V.P.; Makde, R.D.; Kumar, A.; Jangir, R.; Mondal, K.; Haldar, K.K.; Dhayal, R.S. Inorg. Chem 2022, 61, 13342–13354. DOI: https://doi.org/10.1021/acs.inorgchem.2c01281. (c) Kumar, P.; Khirid, S.; Jangid, D.K.; Nishad, C.S.; Chauhan, P.; Kumari, P.; Meena, S.; Bose, S.K.; Kumar, A.; Banerjee, B.; Dhayal, R.S. Inorg. Chem. 2024, 63, 13724–13737. DOI: https://doi.org/10.1021/acs.inorgchem.4c02062. (d) Jangid, D. K.; Dastider, S. G.; Mandal, S.; Kumar, P.; Kumari, P.; Haldar, K. K.; Mondal, K.; Dhayal, R.S. Chem. Eur. J. 2024, e202402900. DOI: https://doi.org/10.1002/chem.202402900.
5. Yusuf, T.L.; Quadri, T.W.; Tolufashe, G.F.; Olasunkanmi, L.O.; Ebenso, E. E.; van Zyl, W.E. RSC Advances 2020, 10, 41967-41982. DOI: https://doi.org/10.1039/D0RA07770D.
6. Sağlam, E.G.; Akkoç, S.; Zorlu, Y.; Bulat, E.; Akgün, A. Polyhedron, 2021, 199, 115097. DOI: https://doi.org/10.1016/j.poly.2021.115097.
7. Aydin, A.; Dede, B. Acta Phys. Pol. A 2023, 144, 154-162. DOI: https://doi.org/10.12693/APhysPolA.144.154.
8. Nizamov, I.S.; Yakovlev, A.A.; Nizamov, I.D.; Terenzhev, D.A.; Ivshin, K.A.; Kataeva, O.N.; Shulaeva, M.P.; Pozdeev, O.K. Appl. Organomet. Chem. 2018, 32, e4320. DOI: https://doi.org/10.1002/aoc.4320.
9. Sosa-García, D.; López-Cardoso, M.; Tlahuext, H.; Vargas-Pineda, G.; Román-Bravo, P.; Villamil-Ramos, R.; Acevedo-Quiroz, M.; Said Razo-Hernández, R.; Gómez-Sandoval, Z.; Alvarez-Fitz, P.; Cea-Olivares, R. Inorg. Chim. Acta 2019, 495, 118943. DOI: https://doi.org/10.1016/j.ica.2019.05.042.
10. Jain, V.K. Coord. Chem. Rev. 1994, 135-136, 809-843. DOI: https://doi.org/10.1016/0010-8545(94)80083-9.
11. (a) Fild, M.F.; Krueger, O; Silaghi-Dumitrescu, I.; Thoene, C.; Weinkauf, A. Phosphorus Sulfur Silicon Relat. Elem. 2007, 182, 2283-2310. DOI: https://doi.org/10.1080/10426500701429122. (b) Hernandez-Galindo, M. del C.; Moya-Cabrera, M.; Jancik, V.; Toscano R.A.; Cea-Olivares R. J. Organomet. Chem. 2016, 813, 55-60. DOI: https://doi.org/10.1016/j.jorganchem.2016.04.005. (c) Baum, R. R.; Veach, J. J.; Semeniuc, R.F.; Wheeler, K.A.; Pellechia, P.J. Inorg. Chim. Acta 2017, 455, 52-60. DOI: https://doi.org/10.1016/j.ica.2016.10.006. (d) Nizamov, I.S.; Gabdullina, G.T.; Nizamov, I. D.; Nikitin, Y.N.; Al'metkina, L.A.; Lyubov, R.; Cherkasov, A. Phosphorus Sulfur Silicon Relat. Elem. 2010, 185, 732-742. DOI: https://doi.org/10.1080/10426500902930142.
12. (a) Ikonen, E. Nature Reviews Molecular Cell Biology, 2008, 9, 125–138. DOI: https://doi.org/10.1038/nrm2336. (b) Lingwood, D.; Simons, K. Science, 2010, 327, 46–50. DOI: https://doi.org/10.1126/science.1174621. (c) Simons, K.; Ikonen, E. Nature, 1997, 387 569–572
13. Van Zyl, W.E.; Fackler J.P. Phosphorus, Sulfur Silicon Relat. Elem. 2000 167 117-132. DOI: https://doi.org/10.1080/10426500008082393.
14. (a) Agilent, CrysAlis PRO, Agilent technologies ltd, begbroke, England. 2014, (b) Sheldrick, G.M. Acta Crystallogr. A., 2008, 64, 112-122. DOI: https://doi.org/10.1107/S0108767307043930. (c) Sheldrick G. M. Acta Crystallogr. C. 2015, 71, 3-8. DOI: https://doi.org/10.1107/S2053229614024218. (d) Speck A.L. Acta Crystallogr. D. 2009, 65, 148-155 DOI https://doi.org/10.1107/s090744490804362x. (e) Westrip, S. P. J. Appl. Crystallogr. 2010, 43, 920-925. DOI: https://doi.org/10.1107/s0021889810022120.
15. Rios, J.L.; Recio, M.C.; Villar A. Ethnopharmacol. 1988, 23, 127-149. DOI: https://doi.org/10.1016/0378-8741(88)90001-3.
16. (a) Haiduc, I.; Silaghi-Dumitrescu, I.; Grecu, R.; Constantinescu, R.; Silaghi-Dumitrescu, L. J. Mol.Struct. 1984, 114, 467–470. DOI: https://doi.org/10.1016/0022-2860(84)87188-4
17. Glidewell, C. Inorg. Chim. Acta 1977, 25, 159-163. DOI https://doi.org/10.1016/S0020-1693(00)95706-2.
18. (a) Martínez García, J.C.; Montes, Tolentino P.; Hernández Ahuactzi, I.F.; Godoy Alcantar C.; Ariza-Castolo, A.; Guerrero Alvarez, J.A. J. Mol. Struct. 2020, 1209, 127915. DOI: https://doi.org/10.1016/j.molstruc.2020.127915. (b) Wrackmeyer, B. Annu. Rep. NMR Spectrosc. 1985, 16, 73 (c) Wrackmeyer B., in: Organotin chemistry in: G.A. Webb (Ed.), Modern Magnetic Resonance, Springer, Dordrecht, 2008.
19. (a) Clark, H.C.; Jain, V.K.; Mehrotra, R.C.; Singh, B.P.; Srivastava, G.; Birchall, T. J. Organomet Chem. 1985, 219, 385-394. DOI: https://doi.org/10.1016/0022-328X(85)87036-4. (b) Otera, J. J. Organomet. Chem. 1981, 221, 57-61 DOI https://doi.org/10.1016/S0022-328X(00)81028-1.
20. James, B.D.; Magee, R.J.; Patalinghug, W.C.; Skelton, B.W.; White, A.H. J. Organomet. Chem. 1994, 64, 51-55. DOI: https://doi.org/10.1016/0022-328X(94)88007-7.
21. Cordero, B.; Gómez, V.; Platero-Prats, A.E.; Revés, M.; Echeverría, J.; Cremades, E.; Barragán, F.; Alvarez, S. Dalton Trans. 2008, 2832-2838. DOI: https://doi.org/10.1039/b801115j.
22. Haiduc, I. Coord. Chem. Rev. 1997, 158, 325-358. DOI: https://doi.org/10.1016/S0010-8545(97)90063-1
23. Addison, A.W.; Rao, T.; Nageswara, R.; Reedijk, J.; Jacobus, V.R.; Verschoor, G.C. J. Chem. Soc., Dalton Trans. 1984, 1349-1356. DOI: https://doi.org/10.1039/DT9840001349.
24. (a) Kumar, S.B.; Chaudhury, M. J. Chem. Soc. Dalton Trans. 1992, 3439-3443. DOI: https://doi.org/10.1039/DT9. (b) Tiekink, E. R. T. Appl. Organomet. Chem. 2008, 22, 533-550. DOI: https://doi.org/10.1002/aoc.1441. (c) Tarassoli A.; Asadi, P.B.; Hitchcock, P.B. J. Organomet. Chem. 2006, 691, 1631-1636. DOI: https://doi.org/10.1016/j.jorganchem.2005.11.060.
25. Van Der Walt, H.; Muller, A.; van Zyl, W.E. Acta Crystallogr. Sect. E Struct. Rep. Online. 2010, 66, 2146. DOI: https://doi.org/10.1107/S1600536810029703.
26. Wolf, S.K.; Grimwood, D.J.; McKinnon, J.J.; Turner, M.J., Jayatilaka D., Spackman, M A. Crystal Explorer ver, 3.1, University of Western Australia Perth, 2013.
27. (a) Gielen, M.; Biesemans, M.; Willem, R. Appl. Organomet.Chem. 2005, 19, 440–450. DOI: https://doi.org/10.1002/aoc.771. (b) Tiekink, E.R.T. Appl. Organomet. Chem. 2008 22 533–550. DOI: https://doi.org/10.1002/aoc.1441. (c) Pachwania, S.; Devi, J.; Taxak B.; Boora A. Phosphorus Sulfur Silicon Relat. Elem. 2022, 198, 102-113. DOI: https://doi.org/10.1080/10426507.2022.2116637.
28. (a) Antonenko, T.A.; Gracheva, Y.A.; Shpakovsky, D.B.; Vorobyev, M.A.; Mazur, D.M.; Tafeenko, V.A.; Oprunenko, Y.F.; Shevtsova, E.F.; Shevtsov, P.N.; Nazarov, A.A.; et al. Int. J. Mol. Sci. 2023, 24, 2024. DOI: https://doi.org/10.3390/ijms24032024. (b) Shiva Prasad, K.: Shiva Kumar, L.; Melvin Prasad; Hosakere D. Revanasiddappa Bioinorg. Chem. Appl. 2010, 854514. DOI: https://doi.org/10.1155/2010/854514.
29. Becker, K.; Heilmann, C.; Peters, G. Clin. Microbiol. Rev. 2014 27, 870–926. DOI: https://doi.org/10.1128/CMR.00109-13.
30. (a) Ruiz de Gopeguia E. et. al. Enferm. Infecc. Microbiol. Clin. 2011, 29, 339-344. DOI: https://doi.org/10.1016/j.eimc.2011.02.001. (b) de Almeida L. M. et al. Antimicrob. Agents Chemother. 2013, 4082-4083. https://doi: 10.1128/AAC.00437-1.
31. Carvajal-Román, L. F. Caracterización estructural de complejos de triorganoestaño (IV) utilizando un ligante ditiofosfonato con una molécula biológicamente activa (colesterol); Bachelor’s Thesis, Universidad Autónoma del Estado de Morelos. http://riaa.uaem.mx/handle/20.500.12055/4494.

Downloads
Published
Issue
Section
License
Copyright (c) 2026 Perla Román-Bravo, Gabriela Vargas-Pineda, Fernando Carvajal-Román, Marcela López-Cardoso, Macdiel Acevedo-Quiroz, Patricia Alvarez-Fitz, Raymundo Cea Olivares

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
Authors who publish with this journal agree to the following terms:
- Authors retain copyright and grant the journal right of first publication with the work simultaneously licensed under a Creative Commons Attribution License that allows others to share the work with an acknowledgement of the work's authorship and initial publication in this journal.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work (e.g., post it to an institutional repository or publish it in a book), with an acknowledgement of its initial publication in this journal.